佰翱得 × SPT Labtech 攻克CryoEM难题,解析 ABCC2 2.51 Å 高分辨率完整结构
2025-11-21
在结构生物学领域,CryoEM(冷冻电镜)是解析生物大分子结构的 “利器”,但样品制备长期以来都是制约分辨率提升的关键瓶颈。近日,佰翱得(Biortus)与 SPT Labtech达成深度合作,通过蛋白工程与先进样品制备技术的创新融合,成功攻克 ABC 转运蛋白 ABCC2 的结构解析难题,获得 2.51 Å 高分辨率完整结构,为膜蛋白研究与药物研发注入强劲动力!
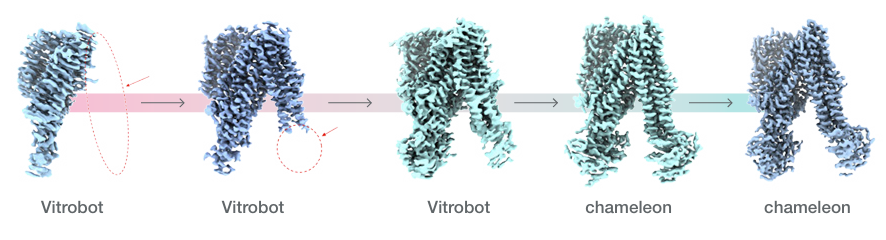
图1:ABCC2 高分辨率结构解析过程
实验难点:CryoEM 样品制备的 “拦路虎”
ABCC2 作为关键跨膜转运蛋白,参与药物代谢、解毒等核心生理过程,其高分辨率结构的解析对药物研发和疾病研究意义重大。但传统 CryoEM 样品制备面临多重挑战:
采用传统制样方法,蛋白易受机械剪切力和空气 - 水界面(AWI)影响,出现结构变性、NBD 结构域缺失等问题;
野生型 ABCC2 样品中,完整双 NBD 结构的颗粒占比极低,导致无法获得蛋白完整全长结构;
即使通过定点突变提升蛋白稳定性,仍有 80% 颗粒存在结构域缺失,难以满足高分辨率解析需求。

图2:ABCC2 常规制样2D结果缺少TMD和NBD domain
亮眼成果:2.51 Å 完整结构的突破
面对这一类蛋白的共性难题,佰翱得与SPT Labtech 发挥各自技术优势,打造 “蛋白工程 + 毫秒样品制备” 的联合解决方案:合作团队通过迭代优化,最终实现关键突破:
样品100%完整性:chameleon 制备的样品中,所有颗粒均保持完整双 NBD 结构,彻底解决传统方法中结构域缺失的问题;
分辨率大幅提升:使用chameleon全自动冷冻制样分辨率从 3.3 Å 逐步提升至 2.51 Å,结构中不仅肽链主链清晰可辨,多个侧链密度也能明确区分;
颗粒分布更优:冷冻时间缩短至200 ms、提高样品浓度后,颗粒在冰层中分布均匀,取向覆盖更全面,为高分辨率重构提供坚实基础。
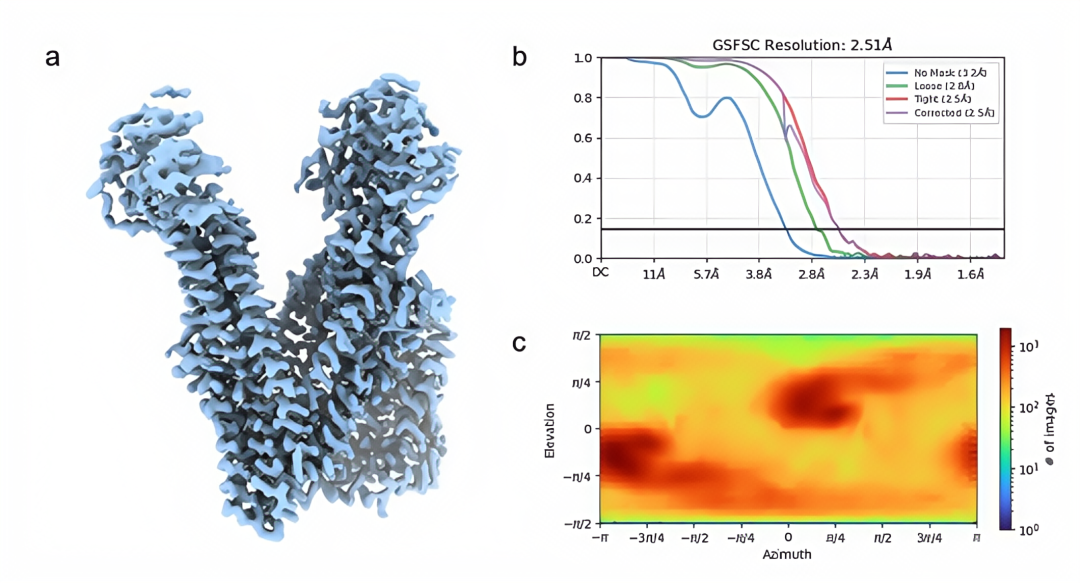
图3:ABCC2(5.5 mg/mL)chameleon 200 ms 制样结果图
对比传统方法,chameleon 系统仅需更少数据量就能实现更高分辨率,充分验证了chameleon冷冻制样的高效性与优越性。相关实验细节也可以点击查看合作发表的英文技术文章。
合作共赢:彰显全链条技术实力
此次合作不仅是技术的成功融合,更是行业资源互补、协同创新的典范。未来,双方将持续深化合作,为更多复杂生物大分子的结构解析提供支持,助力全球生物医药产业发展!
“我们借助 chameleon 的无印迹和超快冷冻技术,成功解决了单颗粒分析中常见的择优取向和 AWI 诱导变性问题。” 佰翱得冷冻电镜高级总监施慧博士表示,“作为专注于结构生物学的CRO,我们期待与 SPT Labtech 深化战略合作,加速客户的药物发现进程。”
SPT Labtech 结构生物学负责人 Paul Thaw 也对合作成果给予高度认可:“与佰翱得这样具有全球影响力的企业合作,助力其突破 workflow 瓶颈,为双方加速药物研发 workflows 的未来奠定了坚实基础。”



